
医疗器械注册医用诊断X射线管组件产品名称可采用《医疗器械分类目录》、国家标准、行业标准中的通用名称医用诊断X射线管组件,或依据《医疗器械通用名称命名规则》命名,例如固定阳极X射线管组件、旋转阳极X射线管组件。
(二)产品的结构和组成
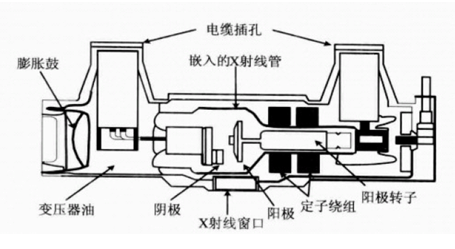
医疗器械产品注册应根据产品实际特点确定结构组成,应描述产品内部关键组件,固定阳极X射线管组件一般由X射线管、X射线保护管套、绝缘油、高压插座、油冷却散热装置(若适用)组成。其中X射线管由阴极、阳极、真空管壳组成。旋转阳极X射线管组件在固定阳极X射线管组件的基础上增加阳极驱动定子等阳极驱动系统。栅控X射线管组件是在固定或旋转阳极X射线管组件的阴极与阳极之间增加一个控制栅极,从而控制阴极灯丝发射电子,即控制X射线的产生。
组成单元结构/功能描述:
X射线管:X射线管内阴极灯丝经灯丝电流加热后,在其周围溢出大量电子云。电子云经由高压电场加速后,形成高能电子束撞击阳极靶盘,产生X射线。
X射线保护管套:保证X射线管周围充满绝缘油,并使绝缘油与空气隔绝。屏蔽由X射线管发出的X射线,只在X射线窗口处敞开。其屏蔽功能由衬在管套内壁的铅层完成。
绝缘油:用于进行高压绝缘和散热使用。X射线管工作时最高对地电压一般有几十或更高千伏,如此高电压是不能暴露在空气中,充斥在X射线管周围的绝缘油对高压进行绝缘,防止击穿。同时高压绝缘油吸收了X射线管产生的热量,通过周围空气流或散热装置进行降温。
高压插座:提供高压连接。
阴极:提供电子源,并使电子聚焦。
阳极:提供电子高速轰击的靶,以发射X射线,并传导和辐射热量。
真空管壳:保证真空密封以提供稳定的真空条件,并有高压绝缘的作用。
阳极驱动定子:用于驱动旋转阳极靶盘旋转。驱动定子为X射线管的旋转阳极提供旋转磁场,推动阳极靶盘旋转。给定子线圈一定频率的电压后,旋转靶盘会以给定的速度旋转,通过靶盘的旋转可以迅速提高靶盘的使用效率。
(三)医疗器械产品注册办理产品工作原理/作用机理
1.工作原理
X射线管组件是利用真空X射线管中高速电子撞击金属靶盘产生X射线的电子器件。当X射线管组件装入X射线影像设备整机中时,由X射线诊断设备整机供给X射线管灯丝电压和阴阳极高压。X射线管灯丝周围产生热电子云,在阴阳极高电压的作用下,热电子云中电子高速飞向阳极,击中阳极靶盘,高速运动的电子与靶盘材料的原子发生相互作用,其动能的一小部分能量转化为辐射能,以X射线的形式释放出,从而对患者被检部位进行曝光,并依靠X射线诊断设备整机对获得图像进行传输,存储和分析。
X射线管组件可分为三大类:
(1)固定阳极X射线管组件的结构相对简单,尺寸较小,阳极靶面固定,适用于热量产生非常低的应用。
(2)旋转阳极X射线管组件的阳极靶面为一个高速旋转的靶盘,从而避免了热量集中产生于固定的焦斑区域内,同样的焦点尺寸可极大地提高X射线管的功率,从而提高影像质量和应用范围。
(3)栅控X射线管组件的栅极上加一定大小的负电位或负脉冲电压(相对阴极灯丝而言),管电流被截止,不发生X射线;负电位或负脉冲消失时,管电流导通,发生X射线。对于栅控X射线管组件,X射线的产生不仅取决于灯丝加热电流和管电压,还取决于栅极电位的变化。由于栅极电压远低于管电压,因此控制相对容易,这意味着产生X射线的过程可以大大缩短,射线中由于过渡过程产生的无用射线比例将大大减少。如果栅极电位采用脉冲电压方式供电,就能实现快速断续X射线摄影。
2.作用机理
因该产品为非直接治疗类医疗器械,故本指导原则不包含产品作用机理的内容。
医疗器械注册办理医用诊断X射线管组件产品注册适用的相关标准如下:
1GB 9706.1-2007医用电气设备第1部分:安全通用要求
2GB 9706.11-1997医用电气设备第2部分:医用诊断X射线源组件和X射线管组件安全专用要求
3GB 9706.12-1997医用电气设备第1部分:安全通用要求并列标准:诊断X射线设备辐射防护通用要求
4GB/T 10151—2008医用X射线设备高压电缆插头、插座技术条件
5YY/T 0291-2016医用X射线设备环境要求及试验方法
6YY/T 0609-2018医用诊断X射线管组件通用技术条件
注:以上标准适用最新版本。
医疗器械注册代办上述标准包括了产品技术要求中经常涉及到的通用标准和方法标准。可根据产品的特点增加相关要求。
产品引用标准的审查可以分两步来进行。首先对引用标准的齐全性、适宜性和准确性来进行审查。此时,应注意标准编号、标准名称是否完整规范,年代号是否有效。
其次是对引用标准的采纳情况进行审查。即所引用的标准中适用的条款要求是否在产品技术要求中进行了实质性的条款引用。这种引用通常采用两种方式:文字表述繁多、内容复杂的可以直接引用标准及条文号;文字比较简单的可以直接引述具体要求。
医疗器械产品注册代办若有新版的强制性国家标准和行业标准发布实施,产品的性能指标要求应执行最新版本国家标准、行业标准的要求。
鸿远医疗器械咨询服务公司是一家技术专业的医疗器械咨询服务公司,专注提供全国各地如:深圳、广州、东莞、中山、佛山、潮州、顺德、广西、上海、西安、重庆、成都、安徽、江苏、浙江等知名城市的医疗器械领域技术咨询服务。鸿远医疗器械咨询专业服务于:医疗器械产品注册证代办理咨询、医疗器械产品分类界定代办理,代办医疗器械生产许可证、一类医疗器械产品备案代办、体外诊断试剂注册、进口医疗器械注册、医疗器械经营许可证代办、二类医疗器械经营备案、CE认证、ISO13485认证、FDA注册、FDA认证、临床试验、医疗器械质量管理体系认证及体系建立与过程确认文件建立( ISO13485, GMP, CE,QSR820,CMDCAS);注册、医疗器械出口销售证明、产品技术要求制订、技术文件、同类产品对比免临床评价资料编写、注册资料编写辅导、医疗器械广告批文申报、电磁兼容整改等提供一站式服务公司,欢迎您咨询与合作!

 在线客服
在线客服