
医疗器械医用电子体温计产品注册临床试验规定:
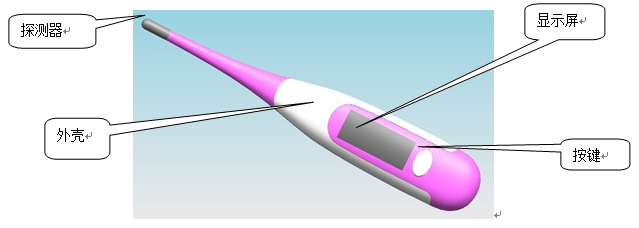
二类医疗器械产品注册 医用电子体温计产品图
临床试验机构应为国家食品药品监督管理部门会同国务院卫生计生部门认定的药品临床试验基地。临床试验应按照《医疗器械临床试验规定》、《医疗器械注册管理办法》附件12及《关于印发豁免提交临床试验资料的第二类医疗器械目录(试行)的通知》(国食药监械〔2011〕475号)的要求进行,企业可进行临床试验或与已上市产品实质性等同对比。对提交的临床试验资料的审查应注意以下要求:
1.注册产品为在境内有已批准同类产品上市的,根据《医疗器械注册管理办法》规定,可提交同类产品对比说明和临床试验资料。
(1)提供与上市同类产品进行实质性等同对比的综述和数据。进行对比并提供数据的内容应当包括但不限于:预期用途、产品结构、工作原理、测量部位、测量方式、主要技术指标、关键部件(探测器、传感器、CPU控制模块)、其他功能等。
(2)提供同类产品临床试验的资料。同类产品临床试验资料包括:该同类产品其原始的临床试验方案和临床试验报告;或者已经公开的,取得广泛认可的临床试验结果并在技术文献资料或医学学术杂志中刊登和记载的,能够证明其安全使用的资料;或者国外同类产品的原始临床试验资料(如果是外文资料,需要译文和原文同时提交)。
2.无法提交同类产品对比说明和临床试验资料,且不在豁免提交临床试验资料的第二类医疗器械目录范围内的,需进行临床试验:
(1)临床试验方案应合理、科学,能够验证产品的预期用途。方案中的临床病例数的确定理由应充分、科学;选择对象范围应明确,涵盖产品的预期用途;临床评价应以体温测量的准确度和精确度作为主要指标;对照品可以是水银体温计或是同类已上市电子体温计,推荐以水银体温计作为对照。
(2)临床试验报告应符合方案的要求。临床试验结果应明确,计量或计数结果可靠,并进行统计学分析;试验效果分析应明确统计结果的临床意义;临床试验结论应明确该产品的预期用途,符合临床试验目的。
深圳鸿远医疗器械咨询服务机构 http://www.yixiezixun.com是一家技术专业的医疗器械产品注册证代办理咨询,医疗器械生产许可证代办,医疗器械经营许可证代办,一类医疗器械产品备案代办,二类医疗器械经营备案,CE认证,ISO13485认证,FDA注册/认证,临床试验,医疗器械质量管理体系认证及体系建立与过程确认文件建立(ISO9001, ISO13485, GMP, CE,QSR820,CMDCAS);注册,出口证,自由销售证办理,临床试验及免临床资料编写,产品技术要求制订,技术文件编写辅导等提供一站式服务公司,欢迎您咨询与合作

 在线客服
在线客服